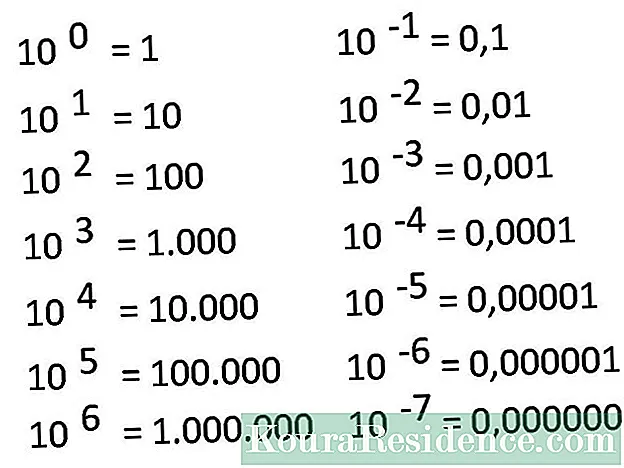Sadržaj
The pH je kratica koja označava vodikov potencijal i djeluje kao mjera kiselosti ili alkalnosti a raspuštanje, koji pokazuje koncentraciju hidronijevih iona prisutnih u otopini.
Pokazalo se da postoji potpuna korelacija između koncentracije vodikovih iona i razine kiselosti a supstancaJake kiseline imaju visoku koncentraciju vodikovih iona, dok slabe kiseline imaju niske koncentracije.
Matematički, pH Definira se kao decimalni logaritam povratne vrijednosti aktivnosti vodikovog iona u otopini. Operacija logaritma koristi se za linearizaciju trenda, tako da broj ima značenje za sebe. Vagu je uveo hemičar Sorenson, koji je vagi dao ime do 1924.
The pH skala je postavljena između broja 0 i 14: 0 je kiseli kraj, dok je 14 alkalni kraj. Broj 7, međuprodukt, je ono što je poznato kao neutralni pH.
Kako se meri?
Za mjerenje pH često se koristi kemikalija jednostavna za upotrebu, a to je Lakmus papir. To je uloga koja mijenja boju ovisno o otopini u koju je uronjen.
Najkiselije tvari će papir pretvoriti u ružičastu, dok će one najosnovnije uzrokovati da plavi. Neki od papira ove vrste imaju oznake razine, tako da tko god ga koristi može jednostavno dekodirati razinu potencijala vodika bojom.
Međutim, uloga Litmusa nije u potpunosti učinkovita, a u slučajevima kada nije učinkovit, uređaj poznat kao pH metar, senzor koji se koristi u hemijskoj metodi za mjerenje pH otopine. Tamo se ćelija za mjerenje pH sastoji od para elektroda, od kojih je jedna napravljena od kalomela, a druga od stakla: ovaj mjerač je vrlo osjetljiv voltmetar, a povezane s njim elektrode stvarat će električnu struju kada su uronjene u otopine.
Primjeri pH određenih tvari
| Sok od limuna (pH 2) | Sok od naranče (pH 4) |
| Želučani sok (pH 1) | Pivo (pH 5) |
| Deterdžent (pH 10,5) | Amonijak (pH 12) |
| Voda sa sapunom (pH 9) | Izbjeljivač (pH 13) |
| Morska voda (pH 8) | Cola soda (pH 3) |
| Krečna voda (pH 11) | Klorovodična kiselina (pH 0) |
| Magnezijevo mlijeko (pH 10) | Baterija (pH 1) |
| Ljudska koža (pH 5,5) | Natrijev hidroksid (pH 14) |
| Mlijeko (pH 6) | Čista voda (pH 7) |
| Sirće (pH 3) | Krv (pH 8) |
Kako održati pH konstantnim?
Ponekad laboratorijski postupak zahtijeva pripremu i skladištenje otopine konstantan pH. Očuvanje ove otopine teže je od njezine pripreme, jer ako dođe u dodir sa zrakom, apsorbirat će ugljični dioksid i postat će kiseliji, a ako se skladišti u staklenoj posudi postat će alkalniji zbog učinka nečistoća. odvojena od stakla.
The tampon rješenja su oni koji mogu održati svoj pH stabilan protiv dodavanja relativno malih količina kiseline ili baze moćan.
Otopine ovog tipa pripremaju se sa slabom kiselinom i solju iste kiseline, ili upotrebom slabe baze i soli iste baze. Čak ćelije živih organizama moraju održavati gotovo konstantan pH, za enzimsko djelovanje i metabolički.
Može vam poslužiti: Primjeri kiselina i baza